El ciclo de Krebs paso a paso
El ciclo de Krebs paso a paso
Publicado por Ramón Contreras
El ciclo de Krebs es un proceso central del metabolismo de todos los seres vivos. Puedes leer más sobre su importancia al otro artículo que le dedicamos aquí (próximamente). En este artículo vamos a analizar el ciclo paso a paso viendo las enzimas que la componen, sus sustratos y productos.
El ciclo de Krebs paso a paso:
1. Citrato sintasa: el acetil (grupo de 2 carbonos), procedente de la degradación de moléculas complejas se une a la Coenzima A para entrar al ciclo. El acetil-CoA transfiere el acetil al oxalacetato (molécula de 4 carbonos) para formar una molécula de ácido cítrico (6 carbonos, 6C). Este paso está catalizado por la citrato sintasa y se consume una molécula de agua en el proceso. El citrato que se forma es capaz de impedir la actividad de la citrato sintasa, por lo que hasta que no se acaba el citrato no continúa generándose.
El ciclo de Krebs paso a paso:
1. Citrato sintasa: el acetil (grupo de 2 carbonos), procedente de la degradación de moléculas complejas se une a la Coenzima A para entrar al ciclo. El acetil-CoA transfiere el acetil al oxalacetato (molécula de 4 carbonos) para formar una molécula de ácido cítrico (6 carbonos, 6C). Este paso está catalizado por la citrato sintasa y se consume una molécula de agua en el proceso. El citrato que se forma es capaz de impedir la actividad de la citrato sintasa, por lo que hasta que no se acaba el citrato no continúa generándose.
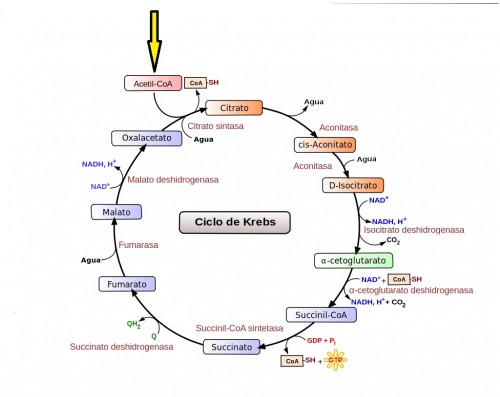
Esquema del ciclo de Krebs
2. A continuación el citrato se convierte en cis-Aconitato (que el mismo enzima catalizara el cambio a isocitrato) mediante la aconitasa. El isocitrato (6 carbonos) es una forma isomérica del citrato, pero sirve como sustrato para el siguiente enzima.
3. La isocitrato deshidrogenasaoxidará el isocitrato a oxoglutarato (6C). En este proceso se genera poder reductor, que será almacenado en un NAD+ que se reducirá a NADH. Esta enzima transforma el isocitrato en oxalsuccinato este cambio modifica la electronegatividad de la molécula, produciéndose una descarboxilación, la rotura de un grupo carboxilo (se elimina en forma de CO2) al perder este carbono se denomina alfa-cetoglutarato o oxoglutarato (con 5 carbonos).
4. La a-cetoglutarato deshidrogenasa transformará el a-cetoglutarato en succinil-CoA (el succinil tiene 4 carbonos) mediante una descarboxilación oxidativa, se pierde otro grupo carboxilo. Este proceso se lleva a cabo en tres pasos, realizados por 3 subunidades del enzima. En este proceso se genera mucha energía, parte de ella servirá para unir una molécula de CoA y el resto se almacena en forma de poder reductor en NAD+, que se convierte en NADH.
5. El succinil-CoA será hidrolizado por la succinil-CoA sintetasa para dar succinil. Esta enzima rompe el enlace entre la conenzimaA y el succil. El cosustrato de esta reacción es el GDP (guanín difosfato) que aprovechará la energía de la reacción para unir un fosforo inorgánico (Pi) y formar GTP.
6. El succinato (4C) es transformado en fumarato (4C) por la succinato deshidrogenasa, la oxidación de la molécula, el poder reductor que se genera se almacena en la FADH2 que almacena menor energía que el NAD+, puesto que esta oxidación no es tan energética.
7. El fumarato mediante la fumarasa es convertido en L-malato mediante la hidratación con un grupo –OH desde una molécula de agua.
8. El malato se oxida por la malato deshidrogenasa dando oxalacetato, generando una última molécula de a NADH. Al final de este paso obtenemos nuevamenteoxalacetato (4C), que puede ser utilizado por el primer enzima del ciclo para volver a generar energía.
El ciclo de Krebs genera poder reductor que será convertido en ATP, la molécula de almacenamiento de energía en la cadena de electrones, lee más de ella aquí (próximamente). En resumen en el proceso se generan dos moléculas de CO2, 3 moléculas de NADH, 1 molécula de GTP y 1 de FADH2 por cada acetil que entra en el ciclo.
ACTIVIDADES:
1.- Imprimir el documento
2.- Realizar el esquema del ciclo de Krebs en el espacio
ACTIVIDADES:
1.- Imprimir el documento
2.- Realizar el esquema del ciclo de Krebs en el espacio






